抽象的な
背景:
光損傷を受けた肌の若返りを目的とした、アブレーション技術と非アブレーション技術を組み合わせた複数の治療法が開発されています。モノポーラ高周波(RF)は、真皮に均一な熱を制御された深さまで届ける、より穏やかで非アブレーションの肌引き締め装置として注目されています。
客観的:
光老化の治療における非切除RFデバイスの臨床効果を評価し、組織学的変化を客観的に定量化しました。
方法:
フィッツパトリック分類III~IV型およびグロガウ分類I~II型のシワを有する6名の被験者に対し、3ヶ月間の治療(2週間間隔で6回のセッション)を実施しました。治療開始前、治療開始後3ヶ月、および6ヶ月の時点で、標準写真および皮膚生検標本を採取しました。コンピュータによる組織計測法および免疫組織化学法を用いて、総エラスチン、I型およびIII型コラーゲン、そして新たに合成されたコラーゲンの定量評価を行いました。盲検化後の写真は、シワの改善について個別にスコア付けしました。
結果:
RF治療は顕著な臨床効果をもたらし、高い満足度とそれに伴う顔面皮膚の改善が見られました。ベースラインと比較すると、治療終了時および治療3ヶ月後において、I型コラーゲン、III型コラーゲン、および新規合成コラーゲンの平均値は統計的に有意に増加しましたが、総エラスチンの平均値は有意に減少しました。
制限事項:
この研究の限界は患者数が少ないことですが、結果は大きな改善を示しています。
結論:
アブレーション治療ほど目覚ましい成果は得られないかもしれませんが、RF は副作用やダウンタイムが少なく、光老化に対する有望な治療オプションです。
キーワード:コラーゲン、エラスチン、非切除、高周波、皮膚老化
皮膚に影響を及ぼす老化プロセスは、臨床的および生物学的に異なる 2 つがあります。1つ目は内因性老化、「生体時計」で、ゆっくりとした不可逆的な組織変性によって皮膚に影響を及ぼします。1 2つ目は外因性老化、「光老化」で、1986 年に初めて、主に紫外線などの環境要因への慢性的な曝露が皮膚に及ぼす影響として説明されました。2 - 4光損傷を受けた皮膚の組織学的および超微細構造的な特徴は、乳頭層と真皮中部に弾性物質が蓄積することであり、これは日光弾性線維症として知られています。5 真皮の全乾燥重量の 80% 以上を占めるコラーゲンは、分解が促進され、ネットワーク形成が減少することで乱雑になります。6 これらの変化が皮膚のたるみやしわの原因となります。7
過去 5 年以上にわたり、多種多様なレーザーやその他の光ベースのシステムが開発され、光損傷や加齢に伴うシワを回復させる能力が評価されてきました。このプロセスは光若返りと呼ばれています。7、8アブレーションレーザーは光損傷を受けた肌の若返りのゴールド スタンダードですが、その使用には重大な副作用と、治療後の長く不快なダウンタイムが伴います。9そのため、近年、アブレーション治療への関心は薄れ、非アブレーションによる肌の若返りが魅力的な代替治療となっています。10 非アブレーション レーザー モダリティは、表皮を損傷することなく真皮に好ましい変化をもたらすように設計されています。ただし、レーザー光は回折、吸収、または散乱するため、放出されたエネルギーのごく一部しか問題となるターゲットに到達しません。その結果、効果は比例して減少します。11 モノポーラ高周波 (RF) 装置は光ではなく電流を生成する点で美容用レーザーとは異なります。生成されるエネルギーは、組織の回折や表皮メラニンによる吸収によって減少する傾向がありません。そのため、RFベースのシステムはあらゆる肌タイプに適しています。12モノポーラRF療法は、真皮層に制御された深さで均一な熱を照射し、コラーゲンを直接収縮させ、即座に肌を引き締めます。8 , 13その後、コラーゲン束の再構築と再配向、そして新しいコラーゲンの形成は、治療後数ヶ月かけて達成されます。14本研究の目的は、光老化の非切除治療としてのモノポーラRF装置の効果を評価し、顔面皮膚の組織学的反応を客観的に定量化し、複数回の治療が臨床結果を改善するかどうかを評価することです。
方法
研究対象集団
この研究は、顔の皮膚のたるみやしわの改善を希望する 6 人の女性ボランティアのコホートで実施されました。年齢は 47 歳から 62 歳まで、平均年齢は 51.1 ± 5.5 歳で、エジプトのアルミニヤにあるアルミニヤ大学病院の皮膚科外来から募集されました。治療と研究の詳細は被験者に十分に説明され、全員がインフォームド コンセント書に署名しました。ボランティアは、フィッツパトリック皮膚タイプ III ~ IV、グロガウ スケールに基づくクラス I ~ II のしわがありました。包含基準には、日光による両側の顔の変化が含まれていました。除外基準は、妊娠または授乳中、日光に対する光線過敏症、感染症または炎症性皮膚疾患の兆候、肥厚性瘢痕またはケロイドの病歴、過去12か月以内の経口イソトレチノインの使用、および顔面領域の以前の皮膚若返り処置でした。
デバイスとテクニック
我々は、RFジェネレータ、コンピュータ制御の自動抵抗テスト技術、連続冷却システム、および3cm²のチップで構成されるモノポーラRF皮膚引き締め装置(Biorad社、深圳GSD Tech Co社、中国広東省)を使用した。RFジェネレータは6MHzの交流電流を発生し、皮膚に電界を形成し、電流の流れに対する抵抗によって組織を加熱する。ThermaCool装置(Solta Medical Inc社、カリフォルニア州ヘイワード)と我々のRF装置の物理的特性(周波数ジェネレータ、電界極性の周波数、エネルギー出力など)は同一である。両装置は、治療エネルギーを伝達するために、伝導結合ではなく容量結合を用いている。伝導結合は、電極の先端に集中するエネルギーに基づいており、その結果、電極と接触する皮膚表面に発生した熱が蓄積され、表皮損傷を引き起こす可能性がある。容量結合は、皮膚表面全体にエネルギーを分散させることで、温度上昇領域を作り出す。10 , 12
簡単に説明すると、局所麻酔クリーム(リドカイン 5%)を治療部位に厚く塗布し、90 分間閉塞したままにした後、クリームを静かに取り除き、患者を治療体位にしました。均一なエネルギー伝導を確保し、治療チップと皮膚との間の熱および電気接触を強化するために、導電性カップリング液を治療部位に塗布しました。コラーゲンの均一な収縮を可能にするために、顔全体に 150 J の初期パスを 2 回実行しました。眼窩周囲、鼻唇溝、額の領域には、200 J の追加パスを 3 回以上実行しました。各セッションでは、治療部位あたりのパスの総数は、顔全体にわたる最初の 2 回のパスと、治療領域をターゲットにした 3~6 回のパス(治療領域あたり合計 5~8 回のパス)で構成されていました。これらのデータを表 Iに示します。パス間に少なくとも 3 分間は皮膚が適切に冷却されるように、パルスの重複は避けました。各セッション中、私たちはボランティアの不快感や耐えられないほどの暑さを監視しましたが、誰も浮腫や暑さによる不快感の兆候を経験しませんでした。
表I.
各セッションの治療エリアごとのボランティアごとのパス数
| 治療面積(200 J) |
||||||
|---|---|---|---|---|---|---|
| 眼窩周囲 |
鼻唇溝 |
|||||
| n = 6 | 顔全体(150 J) | R | L | R | L | 額 |
| 5 | 2 | 3 | 3 | 3 | 3 | 3 |
| 1 | 2 | 3 | 3 | 3 | 3 | 6 |
L 、左; R 、右。
治療計画とフォローアップ
ボランティアは合計3ヶ月間の治療を受けました(2週間間隔で6回のセッション)。各セッション後はアイスパックの使用を避けるよう指示されました。また、真皮内の治癒反応を促進し、コラーゲンの生成を促進するため、日焼け止めを使用して日光への曝露を避けました。写真は各セッションの前後、そして治療3ヶ月後に撮影されました。パンチ生検標本(3mm)は、ベースライン、治療終了時、そして治療3ヶ月後に顔面皮膚から採取されました。治療後の生検標本は、治療前の生検標本に近い部位から採取されました。
組織学的染色と測定
組織は10%緩衝ホルマリンで固定し、パラフィン包埋後、 5µm厚の切片に作製した。組織学的および免疫組織化学的染色、評価、研究はすべて、ペンシルベニア州フィラデルフィアのトーマス・ジェファーソン大学皮膚科・皮膚生物学部で実施した。標準ヘマトキシリン・エオシン染色、Verhoeff-van Gieson染色(弾性線維)、およびピクロシリウスレッド染色(Direct Red 80、Sigma社、ミズーリ州セントルイス)(コラーゲン)を実施した。表皮の厚さは、網隆部の最上部(顆粒細胞層の上部)から最下部(真皮表皮接合部)まで測定した。コンピュータ制御のソフトウェア解析装置を用いて、組織ごとに5回の測定値を算出した。ピクロシリウスレッドは、円偏光照明用フィルターを装備した顕微鏡(Nikon社、ニューヨーク州メルビル)を用いて評価した。免疫組織化学染色およびピクロシリウスレッド染色は、コンピューターベースのソフトウェア (Image-Pro Plus、Media Cybernetics Inc、Silver Spring、MD) を使用して定量化されました。
免疫組織化学染色
総エラスチン、I型およびIII型コラーゲンについて免疫組織化学染色を実施した。ホルマリン固定パラフィン包埋組織スライドを60℃で30~60分間加熱した。その後、組織を100%キシレン(5分間、3回)、100%エタノール(5分間、2回)、95%エタノール(5分間、2回)、75%エタノール(2分間)、50%エタノール(2分間)、蒸留水(H 2 O)(2分間)で脱パラフィン処理した。抗原賦活化は、0.1 mol/Lクエン酸ナトリウム(pH 6.0)中でマイクロ波法により5分間行った。内因性ペルオキシダーゼ活性を阻害するため、組織を脱イオン水中の3%過酸化水素で室温(RT)で10分間インキュベートした。内因性ビオチン活性は、アビジン/ビオチンブロッキングキット(SP-2001、Vector Laboratories、カリフォルニア州バーリンゲーム)を用いてブロックした。切片はブロッキングバッファー(5%正常ヤギ血清、1%ウシ血清アルブミン[BSA]、および0.02%トリトン-X-100[TX-100]をリン酸緩衝生理食塩水[PBS]に溶解したもの)中で室温で60分間ブロッキングした。組織は、エラスチン抗体(1:300; E4013; Sigma)、I型コラーゲン抗体(1:400; sc-59772; Santa Cruz Biotechnology、カリフォルニア州サンタクルーズ)、およびIII型コラーゲン抗体(1:600; ab6310; Abcam、マサチューセッツ州ケンブリッジ)とともに4℃で一晩インキュベートした。 PBSで30分間洗浄した後、組織をビオチン化二次抗体(1:200、PK-6102、Vector Laboratories)とともに室温で60分間インキュベートし、続いてABC試薬(Vectastain Elite ABCペルオキシダーゼキット マウス、PK-6102、Vector Laboratories)とともに室温で30分間インキュベートした。切片はDAB色素基質キット(K3468、Dako、Real Carpinteria、CA)で2~5分間染色し、その後ヘマトキシリン(7211、Thermo Fisher Scientific、Waltham、MA)で対比染色した。スライドはPermount(sp15–100、Thermo Fisher Scientific)でマウントし、顕微鏡(Eclipse TE2000-U、Nikon)で観察した。デジタル画像はEvolution MPカメラ(Media Cybernetics Inc)で収集した。
統計分析
組織学的測定および定量評価は、統計科学ソフトウェアパッケージ(SPSS for Windows、バージョン16、SPSS Inc、シカゴ、イリノイ州)を用いて解析した。統計解析は、一元配置分散分析、ウィルコクソンの対応のあるペアの符号付き順位検定、およびχ2検定を用いて実施した。データは平均値±標準偏差で表した。統計的有意性は、 P値が0.05以下と定義した。
結果
臨床評価
6人のボランティア全員が単極RF試験を完了し、眼窩周囲と額部の皮膚の引き締めとシワの明らかな臨床的改善が見られました(図1、A )。各エンドポイント(治療前、終了時、治療3か月後)で、ボランティア、医師2名、および独立した観察者2名に、シワの改善、皮膚の引き締めと質感、および全体的なボランティアの満足度という以下の基準を評価するよう依頼しました。評価は5段階評価(なし=0%、軽度=1〜25%、中等度=26〜50%、良好=51〜75%、非常に良好=76〜100%)で評価されました。得られた結果は表にまとめられ、ピアソンのχ2検定で統計的有意性についてベースラインと比較されました。ボランティアの評価率は図1、Bに示されています。治療終了時、被験者は肌の引き締めが35~40%改善( P = .02)、肌のきめが30~35%改善( P = .04)、しわが40~45%改善( P = .01)、ボランティア満足度が85~90%改善( P = .001)を示しました。治療3ヶ月後には、被験者間で有意差が認められ、肌の引き締めが70~75%改善(P = .001)、肌のきめが65~70%改善(P = .002)、しわが90~95%改善( P = .0001)、ボランティア満足度が90~95%に上昇( P = .0001)しました。医師および観察者の評価率に関しては、得られたデータはボランティアによる評価率と同等でした。 χ2検定では、各基準においてベースラインと比較して統計的に有意な変化が認められました。さらに、紅斑、浮腫、色素減少または色素沈着といった潜在的な副作用は、4段階評価(なし、軽度、中等度、重度)で評価されました。4回目の施術から2日後に、1名の被験者に軽度の紅斑と軽度の一時的な色素沈着が見られましたが、5日後には治まりました(図1、C )。瘢痕形成は認められませんでした。
図1.
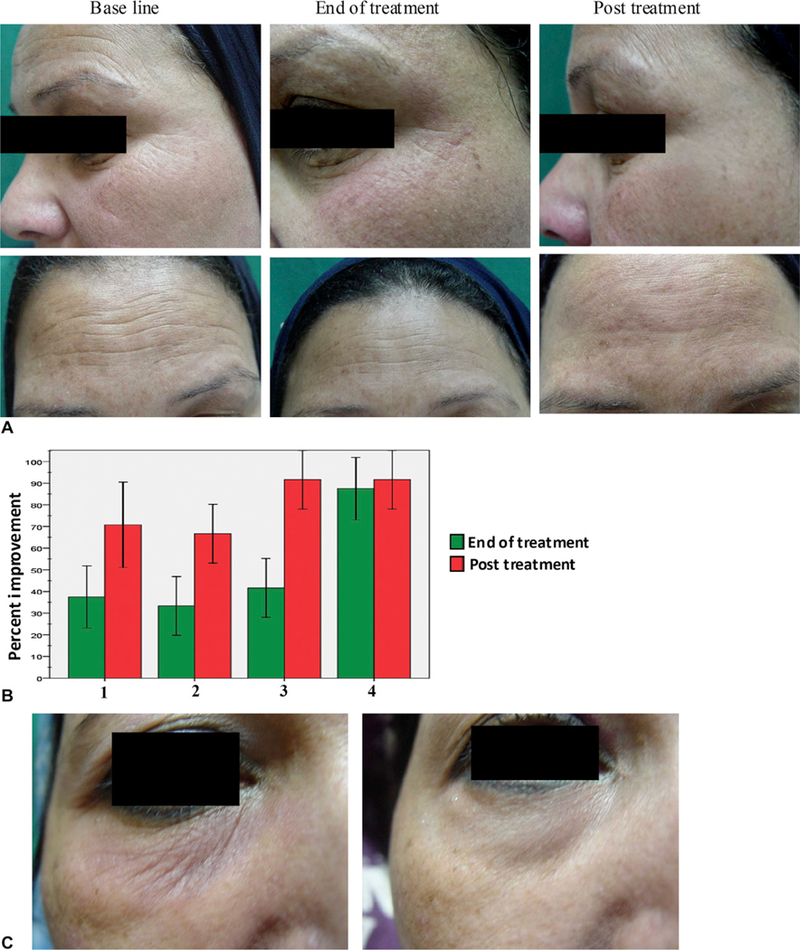
モノポーラ高周波治療に対するボランティアの臨床評価。A 、ベースライン、治療終了時、および治療後 3 か月の眼窩周囲および額部の代表写真。B 、ボランティアの評価率は、ベースラインと比較した治療終了時 (緑) および治療後 3 か月 (赤) の皮膚の引き締め (レーン 1 )、皮膚の質感 (レーン 2 )、しわ (レーン 3 )、および全体的な満足度 (レーン 4 ) の平均パーセント改善を示しています。C 、1 人のボランティアは、4 回目のセッションの 2 日後に軽い紅斑と軽度の一時的な色素沈着を起こしましたが (左)、5 日後に治まりました (右)。
表皮の変化を示す組織学的評価
ヘマトキシリン・エオシン染色切片の顕微鏡的観察では、治療終了時に表皮増殖が認められ、治療3ヶ月後も増加し続けました(図2 )。その結果、表皮の厚さの平均値は、治療前の62.7 ± 2.4 µmから治療終了時には67 ± 3.9 µmへと有意に増加し( P = .044)、さらに治療3ヶ月後には79.5 ± 9.8 µmへと有意に増加しました( P = .002)(表II )。これは、表皮網(真皮表皮境界の顕著な起伏)の発達を伴う、表皮の全体的な形態学的および構造的改善と関連していました。最後に、顆粒層の厚さは、治療前の6.4 ± 1.1 µmから治療終了時には9.9 ± 1.5 µm 、治療3ヶ月後には17.7 ± 3.1 µmへと増加した(それぞれP = .001、.0001)(表IIおよび図2 )。これは、顆粒層中の細胞数およびサイズの増加に起因すると考えられる。
図2.
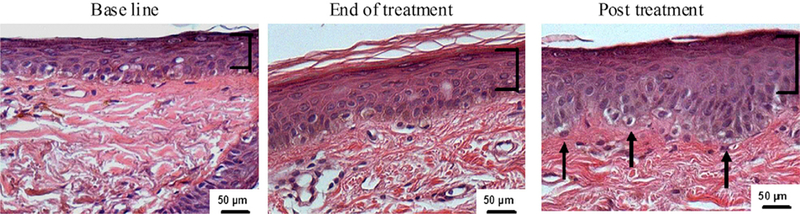
高周波治療は表皮肥大を促進する。皮膚生検標本はホルマリン固定・パラフィン包埋された。組織切片はヘマトキシリン・エオシン染色され、高周波治療後に表皮および顆粒細胞層の肥厚(括弧内)が見られ、網状隆起(矢印)の発達と関連していることが示された。
表II.
表皮および顆粒細胞層の厚さの組織学的分析
| 厚さ、 μm * |
統計的有意性 |
|||||
|---|---|---|---|---|---|---|
| ベースライン | 治療終了 | 治療後3か月 | ベースラインと治療終了時 | 治療終了時と治療後3か月後 | ベースラインと治療後3か月 | |
| 表皮 | 62.7 ± 2.4 | 67 ± 3.9 | 79.5 ± 9.8 | .044 † | .016 † | .002 † |
| 顆粒細胞層 | 6.4 ± 1.1 | 9.9 ± 1.5 | 17.7 ± 3.1 | .001 † | .0001 † | .0001 † |
平均±SD; n = 6。
P≤.05 。
真皮中のエラスチン量の定量
光損傷を受けた皮膚では、結合組織タンパク質エラスチンのレベルが増加し、表皮の下に異常に蓄積して、いわゆる弾性物質を形成します。次に、免疫組織化学染色により、RF治療が真皮全体のエラスチンに与える影響を調べました。ベースラインと比較して、治療後にエラスチンレベルがわずかに低下したことが観察され、治療3か月後にはより顕著になりました(図3、A )。このエラスチン含有量の減少は、太陽由来の弾性物質が表皮から転座したことと関連しており、同時に真皮乳頭層および上部網状層内の正常に見える弾性線維の回復を伴っていました。これらの結果は、コンピューターによる形態計測分析を使用して真皮のエラスチンが占める面積の割合を評価したときに確認されました(図3、B )。 RF治療後、エラスチン染色はベースライン(53.7 ± 7.4%)と比較してわずかに減少しましたが、統計的に有意ではありませんでした(49.9 ± 5.3%、図3 B )。しかし、治療3ヶ月後には総エラスチン量が統計的に有意な減少を示しました(42.2 ± 3.6%、 P = .007)。
図3.
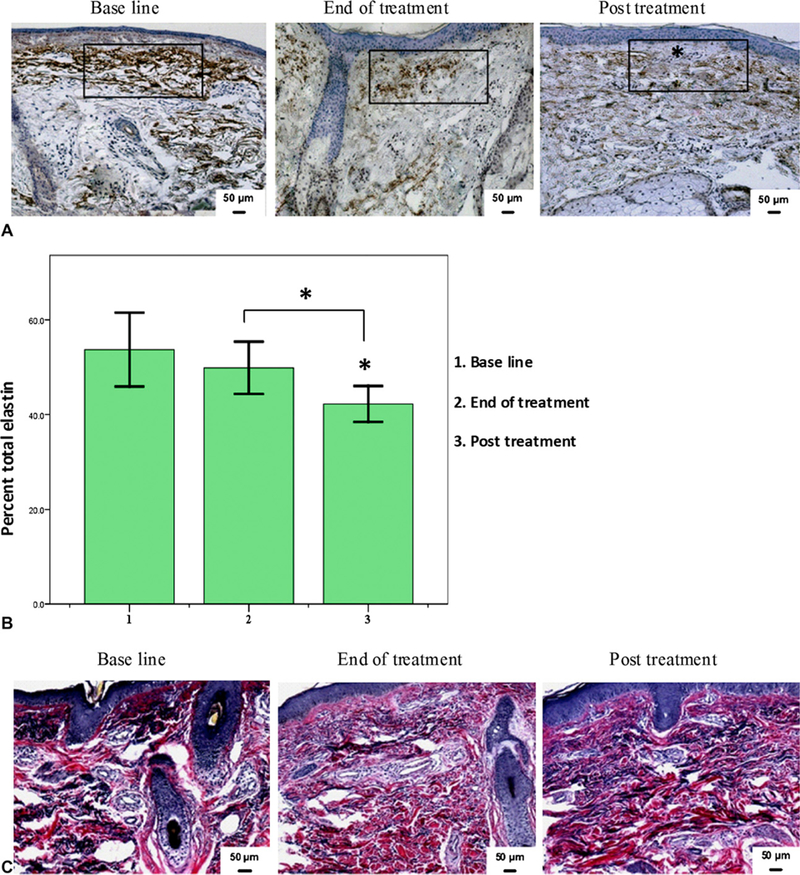
単極高周波治療を受けたボランティアは、真皮エラスチン総量の減少を示しました。A、ベースライン、治療終了時、および高周波治療後の皮膚組織を総エラスチンの免疫染色で検査しました。代表的なサンプルではエラスチン濃度の減少が見られます。エラスチン染色レベルを評価するために、領域(長方形)を使用しました。 *グレンツゾーン。B、治療後に総弾性物質の有意な減少を示すエラスチンが占める真皮の割合。 * P ≤ .05。C、RF治療後の弾性繊維の同様の減少を示す、Verhoeff-van Gieson特殊染色。
これらのエラスチン含量の変化は、フェルホフ・ファン・ギーソン特殊染色によって確認されました(図3、C )。この染色は、弾性組織(青黒から黒)とコラーゲン(赤)を区別するのに有用です。治療後、弾性線維(黒で表示)の含量は客観的に減少し、乳頭層および網状層では正常な弾性線維が回復しました。
真皮におけるコラーゲンの変化の評価
総コラーゲンの免疫組織化学染色(図4、A 、上段)では、治療前のボランティアにおいて、真皮表皮境界部に狭いコラーゲンバンド(グレンツゾーン、9.8 ± 3 µm )が認められました。このコラーゲンバンドは、治療終了時に11 ± 3.6 µmにわずかに増加しました( P = .573)。治療3ヶ月後、皮膚生検標本の染色により、コラーゲンバンドの厚さが15.6 ± 2.3 µmに有意に増加していることが明らかになりました( P = .004)。真皮陽性コラーゲンの割合を定量的に評価したところ、I型コラーゲン(図4、A 、中段)の含有量が治療前の65.8 ± 4.7%から治療終了時には72.2 ± 4.3%( P = .034)、治療後3か月では81.2 ± 4.5%( P = .0001)と、有意に増加しました。最後に、III型コラーゲンの評価では、ベースラインの60.9 ± 2.5%から治療終了時には66.5 ± 4.4%、治療後3か月では73.6 ± 4.8%(それぞれP = .028とP = .0001)と有意に増加していることが明らかになりました(表IIIと図4、B )。まとめると、私たちのデータは、コラーゲン発現の増強がRF治療後3か月間増加し続けたことを示しています。
図4.
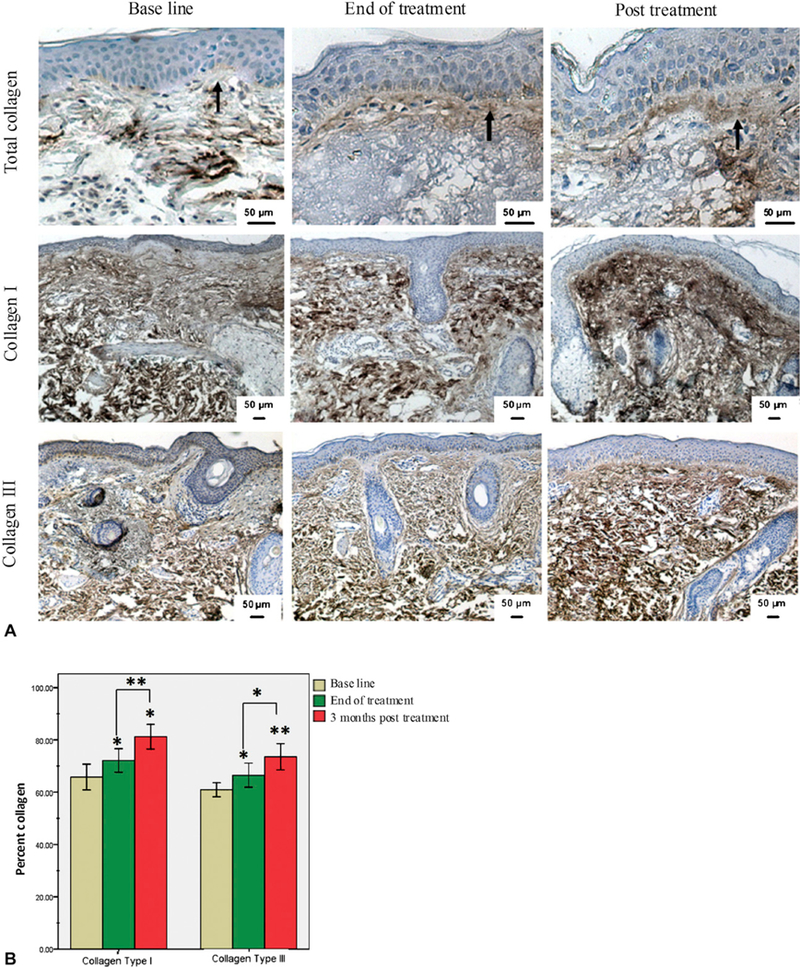
高周波治療に対する真皮コラーゲン含有量の増加。A、ベースライン(左)、治療終了時(中央)、および高周波治療後(右)の皮膚組織の免疫組織化学染色。総コラーゲン(上)およびI型コラーゲン(中央)とIII型コラーゲン(下)。高周波治療後、ベースラインと比較して真皮表皮接合部のコラーゲンバンドの厚さが増加していることが観察された(矢印)。B、コラーゲンレベルを測定し、真皮陽性コラーゲンの割合として値を示した。データは、高周波治療に対するI型コラーゲンとIII型コラーゲンの両方で統計的に有意な増加を示した。* P ≤ .05、** P ≤ .001。
表III.
3つの時点における総エラスチンおよびコラーゲン(新規合成およびI型とIII型)の定量分析
| 相対含有量、% * |
統計的有意性 |
|||||
|---|---|---|---|---|---|---|
| ベースライン | 治療終了 | 治療後3か月 | ベースラインと治療終了時 | 治療終了時と治療後3か月後 | ベースラインと治療後3か月 | |
| 総エラスチン | 53.7 ± 7.4 | 49.9 ± 5.3 | 42.2 ± 3.6 | .324 | .015 † | .007 † |
| 新しく合成されたコラーゲン | 15.3 ± 4.3 | 21.7 ± 3.1 | 26.9 ± 3.7 | .014 † | .024 † | .001 † |
| 総コラーゲンI型 | 65.8 ± 4.7 | 72.2 ± 4.3 | 81.2 ± 4.5 | .034 † | .005 † | .0001 † |
| 総コラーゲンIII型 | 60.9 ± 2.5 | 66.5 ± 4.4 | 73.6 ± 4.8 | .028 † | .023 † | .0001 † |
平均6SD; n = 6。
P≤.05 。
コラーゲンが成熟するにつれ、繊維の光学特性は複屈折(偏光下で色が変わる能力)の増加の兆候を示し、その結果として光の浸透が減少します。組織をピクロシリウスレッドで染色し、偏光顕微鏡で観察すると、太いコラーゲン繊維は赤く染まり、新しく合成された繊維を表す細い繊維は黄色からオレンジ色に染まります。16 , 17免疫組織化学によって観察されたコラーゲンレベルの増加が新しく合成されたコラーゲン形成の増加の結果であるかどうかを評価するために、組織をピクロシリウスレッドで染色しました。結果は、黄色 - オレンジ色の複屈折の存在に反映されるように、新しく合成されたコラーゲン形成の増加を示し、ベースラインの 15.3 ± 4.3% から治療終了時と治療 3 ヵ月後にはそれぞれ 21.7 ± 3.1% と 26.9 ± 3.7%( P = .014 と .001)に有意に増加しました(表 IIIと図 5 )。
図5.
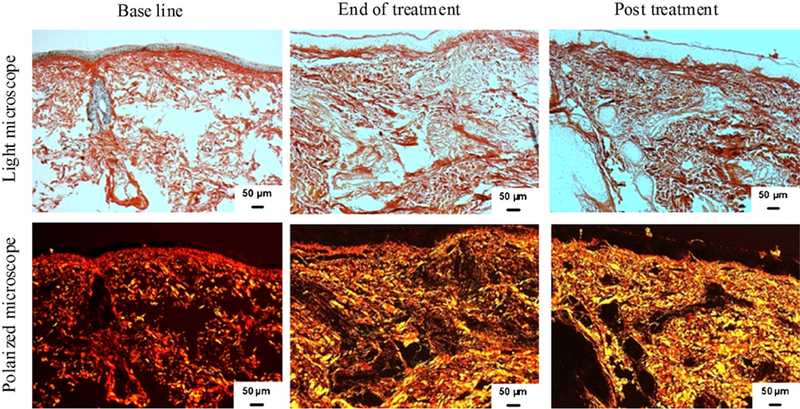
高周波治療による新規合成コラーゲン量の増加。ピクロシリウスレッドで染色した皮膚組織の代表例を明視野(上)と偏光視野(下)で観察した。明視野では総コラーゲン量を捉えている。偏光では黄色からオレンジ色の複屈折が見られ、黄色は新規合成コラーゲン、赤色は総コラーゲンを反映している。高周波治療後の黄色に反映された新規合成コラーゲンの増加に注目。
議論
顔の若返りは発展途上の芸術であり、科学でもあります。長年、光老化した肌の治療と老化の兆候の逆転は、目覚ましい成果が得られることから、アブレーション レーザー リサーフェシング技術に重点が置かれてきました。18最近では、合併症の可能性、回復に長い時間を要すること、最適な結果を維持するために日光への曝露を避ける必要があることが、アブレーション リサーフェシングの魅力を低下させる理由となっています。19現在では、ダウンタイムと合併症を最小限に抑えて肌を若返らせるために使用される、皮膚老化に対する幅広い非アブレーション治療への関心が高まっています。7非アブレーション若返りに関するすべての研究の基本的な問題は方法論に関連しています。しわの深さや皮膚の弾力性の研究に対する標準的かつ客観的なアプローチがほとんどないためです。臨床結果は最終的に、医師、ボランティア、またはその両方の主観的な観察に依存します。また、写真による記録は、治療の質と有効性を示すには不十分な方法であることが示されています。 20 – 22この研究では、モノポーラ RF が肌の引き締めと外観に及ぼす影響を客観的に評価する手段という文脈の中で、主観的評価を改善することを目的としました。これは、組織化学および免疫染色技術、ベースライン、治療終了時、治療後 3 か月の皮膚の組織計測的評価によって達成されました。モノポーラ RF は、2002 年にしわと肌の引き締めの非切除治療に対して、2004 年には顔全体の治療に対して食品医薬品局に承認されました。23 , 24多くの研究で、RF は軽度から中程度のしわを伴う、老化の初期兆候がある患者に最適であると報告されています。14 , 25 – 27そのため、この研究は、比較的軽度から中程度の光老化 (Glogau I-II) の被験者に焦点を当てました。私たちの研究では、被験者の臨床結果を評価した結果、治療終了時に顕著な改善が見られ、治療後 3 か月も改善が継続していました。皮膚の引き締めの改善は、治療終了時の 35~40% から、治療後 3 ヵ月で 70~75% に増加しました。顔のしわの出現は、治療終了時の 40~45% から、治療後 3 ヵ月で 90~95% に改善しました。これらの皮膚の機械的特性は、2 つの主な原則 (1) 力を加えて、この歪みによって生じる力の減少を時間に基づいて計算する、(2) 対照的に、皮膚にひねりを加えて、反動時間を測定する、という28に基づくさまざまな臨床方法を使用して客観的に測定することもできます。さらに、皮膚の弾力性と反動を評価するための追加の方法には、吸引チャンバー法、ツイストメトリー、レバーロメトリー、インデントメトリー、ガスベアリング電気力計、ビデオ顕微鏡検査、皮膚チップ技術、および弾動測定法があります。28 – 30 RF デバイスの以前の研究では、著者らは被験者に 1 回の RF 治療を行い、結果を評価しました。 Ruiz-Esparza と Gomez 29 は、1 回の治療と複数回の施術から 3 か月後に、15 人のボランティアのうち 14 人で皮膚の引き締めとほうれい線および眼窩周囲のしわが最大 50% 改善したことを発見しました。しかし、以前の 2 つの研究では、複数回の施術と複数回の施術で結果が改善する可能性があることが示されています。 30 , 31 Jacobson ら 30 は、24 人の成人患者を ThermaCool システム (Solta Medical Inc) で治療しました。被験者は 1 か月から 3 か月ごとに施術を受けました。研究者らは、この研究で合計何回の施術が適用されたかを特定していませんが、「複数回の施術を受けた患者では、その後の施術でたるみがさらに改善したようだ」と述べています。さらに最近の研究では、Sukal と Geronemus 31が、額に 2 回、頬に 3 回、首に 1 回施術を行い、各患者は 4 週間の間隔をあけて 1 回から 3 回の治療を受けました。著者らは、患者の1か月の追跡調査で目に見える改善が見られ、3か月の追跡調査ではさらに大きな改善が見られたと報告した。
初期の研究では、1回の治療後、複数回の施術の方が1回の施術よりも良好な結果が得られたことが明らかになりました。30さらに、著者らは複数回の施術が1回の施術よりも結果を改善することを実証しました。文献のさらなる調査でも同様の結果が得られています。14、26、30、31
熱による創傷治癒に対する生体内の反応は、炎症、増殖、リモデリングという 3 つの連続した段階から構成されます。3このことが、臨床的に目に見える結果が治療開始後 3~6 か月の間にのみ達成された理由を説明できるかもしれません。光老化した皮膚は、表皮の厚みが減少し、角質隆起が平坦化することを伴います。32観察された RF エネルギーは真皮層をターゲットにしていますが、この研究では、説明をさらに研究する必要がある表皮の組織学的特徴の顕著な変化が観察されました。治療終了時と治療 3 か月後には、特に顆粒細胞層で表皮の厚みが顕著に増加しました (図 2 )。これらの知見は、表皮の細胞増殖が増加し、皮膚の外観の改善に寄与している可能性があることを示唆しています。
特定のクロモフォアをターゲットとするほとんどのレーザーとは異なり、モノポーラ RF の出力エネルギーはクロモフォアに依存せず、主に組織内の水分によって熱に変換されます。その結果、エネルギーは真皮の 3 次元レベルに伝達されます。10熱損傷の深さは表皮の下 100 ~ 400 µm に限定され、組織学的には最も多くの弾性物質が見られる領域です。33 しわに関連する微視的変化は主に真皮で発生します。日光によるダメージを受けた皮膚では、主な真皮の変化は異常な弾性物質の大きな塊が沈着し、通常はコラーゲンが豊富な真皮が置き換わることです。34 この研究では、老化した皮膚で発生する大きな変化の 1 つである総エラスチンに対する RF による変化を評価しました。その結果、治療終了時には総エラスチン含有量に有意な変化は見られず、治療3か月後には弾性組織が有意に減少することが示されました。この減少は、弾性繊維の再配向を伴う弾性物質の下方配置と沈下を伴っていました。弾性繊維の質の改善と日光弾性線維症は、高周波によるコラーゲン形成と新たに合成されたコラーゲンの影響によって説明できます。これらのコラーゲンは、真皮マトリックス繊維の再配向によって弾性物質を置き換えます。弾性繊維の再配向は、適切な集合を伴う新たな弾性繊維の合成を反映している可能性があります。
高周波(RF)によって発生する熱は、コラーゲン分子の三重らせん構造に影響を与え、分子内水素結合を切断することでコラーゲン線維の変性と即時収縮を引き起こすと考えられています。8時間の経過とともに、熱を介した治癒反応として、線維芽細胞が刺激され、新たなコラーゲンの沈着とリモデリングが促進されます。その結果、コラーゲンのさらなる引き締めと、全体的なコラーゲン含有量の増加がもたらされます。11 Bassichisら35 は、単極RFの新たな作用機序の可能性を明らかにしました。皮下脂肪小葉は、コラーゲンをベースとした線維性隔壁の絡み合ったネットワークによって分離されています。RFエネルギーは通常、抵抗が最も少ない経路をたどるため、線維性隔壁が優先的に加熱され、コラーゲン線維の収縮が起こります。35これが、その後の皮下組織のリモデリングと皮膚の引き締めの鍵となり、皮膚は下層構造に接着すると考えられています。36
私たちの研究では、表皮下のコラーゲンの状態から始めて、RF がコラーゲンの含有量と形成に及ぼす影響を評価しました。真皮と表皮の境界にある狭いコラーゲン帯であるグレンツゾーンの厚みがわずかに増加し、治療後 3 ヵ月で厚みが有意に増加したことが分かりました。正常な真皮コラーゲン線維は乾燥重量の約 80% を占め、真皮の引張特性を担っています。真皮コラーゲンは主に I 型 (80%~85%) と III 型 ( 10 % ~15%) コラーゲンで構成されています。5、34 真皮に熱を加えることでしわを軽減する手法は、新しいコラーゲンの形成を刺激することに基づいており、この研究では、真皮コラーゲンの定量評価により、治療終了時に I 型と III 型コラーゲンの両方が有意に増加したことが明らかになりました。これらの結果は、RF 治療後に I 型と III 型コラーゲンが新たに形成されることを実証した過去の研究結果と一致しています。 37 – 39しかし、本研究では、治療後3ヶ月間もI型およびIII型コラーゲンが有意に増加し続けたことが示されました。さらに、RFが新規コラーゲン形成に及ぼす影響、そして免疫組織化学染色で観察されたコラーゲンレベルの増加が、新規合成コラーゲン形成の促進によるものかどうかを評価しました。偏光顕微鏡下でピクロシリウスレッドを用いて新規合成コラーゲンを検出したところ、治療終了時および治療後3ヶ月時点で、ベースラインと比較して新規合成コラーゲンが有意に増加しており、RFが総コラーゲン量と新規コラーゲン形成の両方に良好な反応を示したことを反映しています。
RFチップに備わった保護機構にもかかわらず、4回目の施術から2日後に、1名のボランティアに軽度の紅斑と軽度の一時的な色素沈着が発現しました。この合併症は、治療チップが皮膚表面に不均一に接触し、単一の治療部位にRFエネルギーが蓄積された結果発生した可能性があります。この合併症は再発することなく治まりました。本研究の明らかな限界の1つは、ボランティア数が比較的少なかったことです。それでも、結果はRF治療後の臨床的および組織学的改善の証拠を示しました。これまでの発表では、顔の引き締めなど、RF後の皮膚の変化の改善が示唆されていますが、治療を受けたボランティアの皮膚を組織学的に分析した研究はほとんどありません。8、34、40、41
結論として、モノポーラRFは、光老化した肌を引き締め、若返らせ、顔のたるみを整える効果のある、効果的で価値のある治療法です。この治療法は、比較的リスクが少なく、ダウンタイムもほとんどないという利点を有し、修復プロセスを刺激し、臨床的および組織病理学的に老化の兆候を逆転させます。
カプセル概要。
-
モノポーラ高周波治療は、ダウンタイムをほとんどかけずに光老化した肌を効果的に引き締め、若返らせるために使用できる貴重な治療法です。
-
引き締め効果は、高周波治療終了後も 3 か月間継続するようです。
-
高周波はコラーゲンの合成と含有量を高めることで長期的な効果を示しました。
謝辞
エジプト共和国文化教育局およびエジプト学者プログラム (Dr Medhat)、および国立衛生研究所 R01 AR28450 (Dr Uitto) の支援を受けています。
著者は、この記事の作成に協力してくれたCarol KellyとAlicia Dowlingに感謝します。
脚注
利益相反: なし。
参考文献
- 1. El-Domyati M, Attia S, Saleh F, Brown D, Birk DE, Gasparro F, et al. 内因性老化と光老化:皮膚の組織病理学的、免疫組織化学的、超微細構造的比較研究. Exp Dermatol 2002;11:398–405. [ DOI ] [ PubMed ] [ Google Scholar ]
- 2. Kligman LH, Kligman AM. 光老化の本質:その予防と修復. Photodermatol 1986;3:215–27. [ PubMed ] [ Google Scholar ]
- 3. Helfrich YR, Sachs DL, Voorhees JJ. 皮膚老化と光老化の概要. Dermatol Nurs 2008;20:177–83. [ PubMed ] [ Google Scholar ]
- 4. Uitto J, Fazio MJ, Olsen DR. 皮膚老化の分子メカニズム:真皮における加齢に伴う結合組織の変化. J Am Acad Dermatol 1989;21:614–22. [ PubMed ] [ Google Scholar ]
- 5. Uitto J. 皮膚老化におけるエラスチンとコラーゲンの役割:内因性老化と光曝露. J Drugs Dermatol 2008; 7:s12–6. [ PubMed ] [ Google Scholar ]
- 6. El-Domyati M, Attia S, Saleh F, Ahmad H, Uitto J. 光老化した顔面皮膚に対する局所トレチノインの効果:組織学的、免疫組織学的、および超微細構造学的研究. J Cosmet Dermatol 2004;3:191–201. [ DOI ] [ PubMed ] [ Google Scholar ]
- 7. Kim KH, Geronemus RG. 皮膚若返りのための非切除レーザーおよび光療法. Arch Facial Plast Surg 2004;6: 398–409. [ DOI ] [ PubMed ] [ Google Scholar ]
- 8. Zelickson BD, Kist D, Bernstein E, Brown DB, Ksenzenko S, Burns J, et al. 高周波を用いた非切除型皮膚リモデリングデバイスの効果に関する組織学的および超微細構造的評価:パイロットスタディ. Arch Dermatol 2004;140: 204–9. [ DOI ] [ PubMed ] [ Google Scholar ]
- 9. Alexiades-Armenakas MR, Dover JS, Arndt KA. レーザー皮膚リサーフェシングのスペクトル:非切除型、フラクショナル型、切除型レーザーリサーフェシング. J Am Acad Dermatol 2008;58: 719–37. [ DOI ] [ PubMed ] [ Google Scholar ]
- 10. Atiyeh BS, Dibo SA. 老化皮膚の非外科的非切除治療:積極的なマーケティングとエビデンスに基づく有効性の間の高周波技術. Aesthetic Plast Surg 2009;33:283–94. [ DOI ] [ PubMed ] [ Google Scholar ]
- 11. Ruiz-Esparza J. 顔と首の若返りのための非切除型高周波療法. 重要な部位に熱を集中させることで、より迅速、安全、そして痛みの少ない施術:ThermaLiftコンセプト. J Cosmet Dermatol 2006;5:68–75. [ DOI ] [ PubMed ] [ Google Scholar ]
- 12. Alster TS, Lupton JR. 高周波デバイスを用いた非切除性皮膚リモデリング. Clin Dermatol 2007;25:487–91. [ DOI ] [ PubMed ] [ Google Scholar ]
- 13. Kist D, Burns AJ, Sanner R, Counters J, Zelickson B. 複数パス低エネルギーと単一パス高エネルギーの高周波治療の超微細構造評価. Lasers Surg Med 2006; 38:150–4. [ DOI ] [ PubMed ] [ Google Scholar ]
- 14. Bogle MA, Ubelhoer N, Weiss RA, Mayoral F, Kaminer MS. 下顔面の高周波引き締めにおけるマルチパス・低フルエンスアルゴリズムの評価. Lasers Surg Med 2007;39:210–7. [ DOI ] [ PubMed ] [ Google Scholar ]
- 15. Glogau RG, Matarasso SL. ケミカルピーリング:トリクロロ酢酸とフェノール. Dermatol Clin 1995;13:263–76. [ PubMed ] [ Google Scholar ]
- 16. Rich L, Whittaker P. コラーゲンおよびピクロシリウスレッド染色:偏光光による線維色と空間分布の評価. Braz J Morphol Sci 2005;22:97–104. [ Google Scholar ]
- 17. Whittaker P, Kloner RA, Boughner DR, Pickering JG. ピクロシリウスレッド染色と円偏光を用いた心筋コラーゲンの定量評価. Basic Res Cardiol 1994; 89:397–410. [ DOI ] [ PubMed ] [ Google Scholar ]
- 18. Hirsch RJ, Dayan SH. 非切除的表面再建術. Facial Plast Surg 2004;20:57–61. [ DOI ] [ PubMed ] [ Google Scholar ]
- 19. Carruthers J, Carruthers A. 新型高周波チップによる上眼瞼および下眼瞼の皮膚縮小. Dermatol Surg 2007;33: 802–9. [ DOI ] [ PubMed ] [ Google Scholar ]
- 20. Goldberg DJ, Rogachefsky AS, Silapunt S. 顔面しわの非切除レーザー治療:1450ダイオードレーザーと動的冷却装置を併用した治療と動的冷却装置のみの治療の比較. Lasers Surg Med 2002;30:79–81. [ DOI ] [ PubMed ] [ Google Scholar ]
- 21. Fournier N, Dahan S, Barneon G, Diridollou S, Lagarde JM, Gall Y, et al. 非切除性リモデリング:1540 nm Er:ガラスレーザーの臨床的、組織学的、超音波画像および形状測定による評価. Dermatol Surg 2001;27:799–806. [ DOI ] [ PubMed ] [ Google Scholar ]
- 22. Grema H, Greve B, Raulin C. 顔面しわのサブサーフェシングかリサーフェシングか?レビュー. Lasers Surg Med 2003;32:405–12. [ DOI ] [ PubMed ] [ Google Scholar ]
- 23. De Felipe I, Del Cueto SR, Perez E, Redondo P. 非切除型高周波療法後の副作用:290人の患者の追跡調査. J Cosmet Dermatol 2007;6:163–6. [ DOI ] [ PubMed ] [ Google Scholar ]
- 24. Dover JS, Zelickson B, Burns J, Hughes C, Hugo B, Chan H, et al. 5,700人の患者を対象としたモノポーラ高周波による顔面皮膚引き締め治療の調査結果:低エネルギー・マルチパス法による臨床エンドポイントアルゴリズムの評価. Dermatol Surg 2007;33:900–7. [ DOI ] [ PubMed ] [ Google Scholar ]
- 25. Alster TS, Tanzi E. 非切除型高周波装置による首と頬のたるみの改善:リフトアップ効果の体験. Dermatol Surg 2004;30:503–7. [ DOI ] [ PubMed ] [ Google Scholar ]
- 26. Abraham MT, Vic Ross E. 下顔面および頸部における非切除型高周波若返り療法の最新概念. Facial Plast Surg 2005;21:65–73. [ DOI ] [ PubMed ] [ Google Scholar ]
- 27. Fisher GH, Jacobson LG, Bernstein LJ, Kim KH, Geronemus RG. 顔面たるみに対する非切除型ラジオ波治療. Dermatol Surg 2005;31:1237–41. [ DOI ] [ PubMed ] [ Google Scholar ]
- 28. Léveˆque JL. 皮膚老化の定量的評価. Clin Geriatr Med 2001;17:673–89. [ DOI ] [ PubMed ] [ Google Scholar ]
- 29. Ruiz-Esparza J, Gomez JB. メディカルフェイスリフト:非侵襲性・非外科的アプローチによる顔面皮膚の組織引き締め(非切除高周波療法). Dermatol Surg 2003;29:325–32. [ DOI ] [ PubMed ] [ Google Scholar ]
- 30. Jacobson LG, Alexiades-Armenakas M, Bernstein L, Geronemus RG. 非侵襲性高周波デバイスによる鼻唇溝と頬のたるみの治療. Arch Dermatol 2003;139:1371–2. [ DOI ] [ PubMed ] [ Google Scholar ]
- 31.スカル SA、ジェロネムス RG。サーマクール: 若返りのための非破壊的高周波。クリン・ダーマトール 2008;26:602–7。 [ DOI ] [ PubMed ] [ Google Scholar ]
- 32. Ruiz-Esparza J, Gomez JB. 活動性尋常性ざ瘡に対する非切除性高周波療法:中等度から重度の活動性尋常性ざ瘡の治療における深部真皮温熱療法(温熱療法);22名の患者を対象とした報告. Dermatol Surg 2003;29:333–9. [ DOI ] [ PubMed ] [ Google Scholar ]
- 33. Dierickx CC. 非侵襲性皮膚若返りにおける深部加熱の役割. Lasers Surg Med 2006;38:799–807. [ DOI ] [ PubMed ] [ Google Scholar ]
- 34. El-Domyati M, Attia S, Saleh F, Ahmad H, Uitto J. トリクロロ酢酸ピーリングと皮膚剥離:組織学的、免疫組織学的、超微細構造学的比較. Dermatol Surg 2004;30:179–88. [ DOI ] [ PubMed ] [ Google Scholar ]
- 35. Bassichis BA, Dayan S, Thomas JR. 非切除型高周波装置を用いた顔面上部3分の1の若返り. Otolaryngol Head Neck Surg 2004;130:397–406. [ DOI ] [ PubMed ] [ Google Scholar ]
- 36. Taylor MB, Prokopenko I. 顔面たるみに対する高周波治療と長パルスNd-YAG治療の分割顔比較. J Cosmet Laser Ther 2006;8:17–22. [ DOI ] [ PubMed ] [ Google Scholar ]
- 37. Sarradet MD, Hussain M, Goldberg DJ. 電気外科的リサーフェシング:臨床的、組織学的、電子顕微鏡的評価. Lasers Surg Med 2003;32:111–4. [ DOI ] [ PubMed ] [ Google Scholar ]
- 38. England LJ, Tan MH, Shumaker PR, Egbert BM, Pittelko K, Orentreich D, et al. 動物モデルにおける軟部組織充填剤に対する単極高周波治療の効果. Lasers Surg Med 2005;37:356–65. [ DOI ] [ PubMed ] [ Google Scholar ]
- 39. Fenelon G, Franco M, Mora O, Katchburian E, De Paola AA. ステロイドと抗酸化物質の併用療法は慢性高周波病変周囲の超微細構造損傷を予防する. Pacing Clin Electrophysiol 2004;27:65–72. [ DOI ] [ PubMed ] [ Google Scholar ]
- 40. Burns JA. 「サーマジェイ:モノポーラ高周波療法」Aesthet Surg J 2005;25:638–42. [ DOI ] [ PubMed ] [ Google Scholar ]
- 41. De Felipe I, Redondo P. 非切除型高周波を用いた脂肪萎縮を説明する動物モデル. Dermatol Surg 2007;33: 141–5. [ DOI ] [ PubMed ] [ Google Scholar ]
この記事はhttps://pmc.ncbi.nlm.nih.gov/articles/PMC6541915/から抜粋したものです。

